Sistemas CRISPR-Cas: Revolucionar a tecnologia de edição do genoma

CRISPR-Cas9: desbloquear a edição de precisão do genoma para avanços na medicina, na agricultura e não só.

A descoberta do CRISPR (Repetições Palindrômicas Curta e Regularmente Agrupadas) e suas proteínas Cas associadas revolucionaram a engenharia genética, proporcionando uma precisão e versatilidade sem precedentes. Iniciada pelo trabalho fundamental de Doudna e Charpentier (2012), o CRISPR-Cas9 usa um mecanismo bacteriano de defesa para gerar quebras de fita dupla no DNA, permitindo a edição precisa de genes, incluindo knock-out ou knock-in via reparo mediado por homologia (HDR). Desde então, os sistemas CRISPR se diversificaram, com inovações como base editors, prime editors e CRISPR-interferência (CRISPRi/a) expandindo a caixa de ferramentas da engenharia genética de precisão.
Os sistemas CRISPR-Cas funcionam via um mecanismo em duas etapas, onde o RNA guia (gRNA) leva a endonuclease Cas9 a um local específico do genoma, causando quebras de fita dupla (DSBs) (Zakrzewska e Burmistrz, 2023). Essas quebras são reparadas por meio de fusão de extremidades não-homólogas (NHEJ) ou reparo mediado por homologia (HDR), permitindo a edição genética precisa (Zakrzewska e Burmistrz, 2023). O processo pode ser dividido em três etapas: reconhecimento, clivagem e reparo (Asmamaw e Zawdie, 2021). Inicialmente, o complexo Cas9: sgRNA se liga ao DNA (Bhattacharya e Satpati, 2022). O crRNA maduro é integrado ao complexo efetor e procura sequências que sejam complementares ao seu fragmento espaçador (Zakrzewska e Burmistrz, 2023). Para os sistemas Class 2 Tipo II, o complexo Cas9, juntamente com o crRNA maduro e o tracrRNA, varre o DNA em busca de um motivo adjacente à protospacer (PAM) (Zakrzewska e Burmistrz, 2023). A detecção da sequência complementar induz a estrutura de loop R, levando a uma quebra de fita dupla mediada pelos domínios HNH e RuvC (Zakrzewska e Burmistrz, 2023).
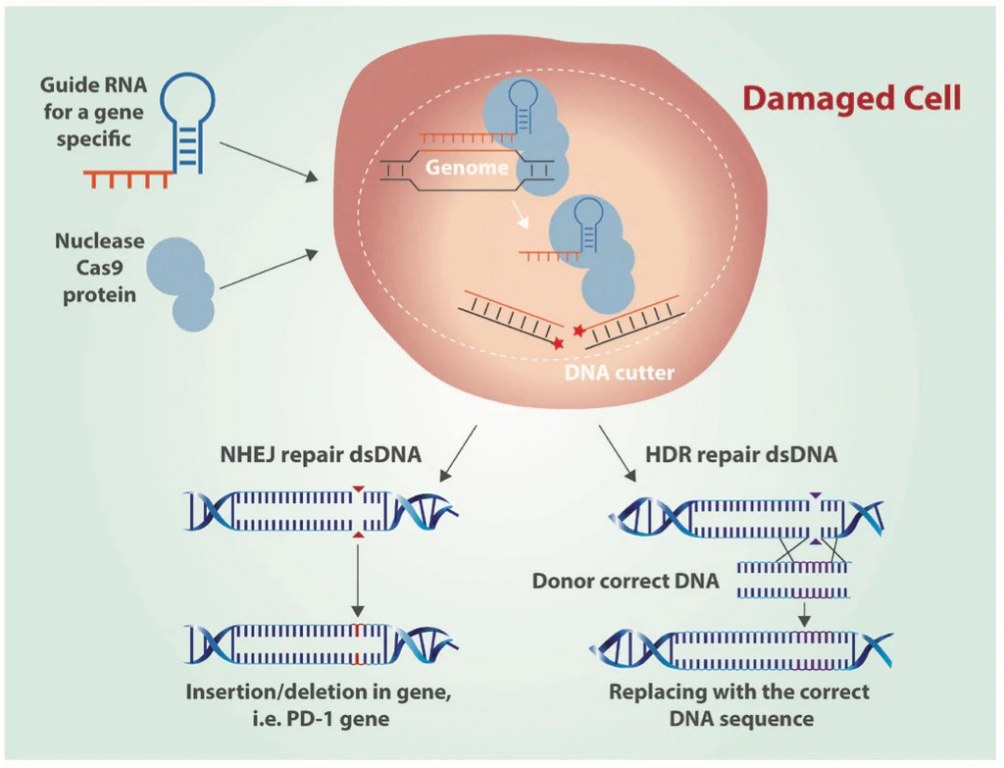
Figura 1: Edição de genes pelo CRISPR Cas9 do DNA com fusão de extremidades não-homólogas (NHEJ) e reparo mediado por homologia (HDR) (Castillo, 2016).
Aplicações
Terapia Gênica
Uma das aplicações mais promissoras da tecnologia CRISPR-Cas é na terapia gênica. Ao corrigir mutações genéticas responsáveis por doenças, os pesquisadores podem abordar esses defeitos diretamente na origem. Exemplos notáveis incluem a edição do gene CCR5 em células T humanas para conferir resistência à infecção pelo HIV (Zhu, 2022). Além disso, o CRISPR tem sido usado para criar modelos de camundongos que imitam doenças humanas, permitindo o estudo dos mecanismos patofisiológicos e das estratégias terapêuticas (Cribbs e Perera, 2017).
Medicina de Precisão
A capacidade do CRISPR de editar genes com precisão abre novas possibilidades para a medicina personalizada. Ao adaptar os tratamentos à composição genética de um indivíduo, o CRISPR pode melhorar a eficácia terapêutica e minimizar os efeitos colaterais. Pesquisas estão, por exemplo, explorando seu uso em terapias contra o câncer, abordando oncogenes e genes supressores de tumor para inibir o crescimento de tumores (Zhu, 2022).
Biotecnologia Agrícola
Além da saúde humana, os sistemas CRISPR-Cas estão revolucionando as práticas agrícolas. A tecnologia permite o desenvolvimento de culturas com características aprimoradas, como resistência a doenças, tolerância à seca e perfis nutricionais melhorados. Esses avanços biotecnológicos prometem ajudar a resolver problemas de segurança alimentar causados pelas mudanças climáticas e pelo crescimento populacional (Zhu, 2022).
Sistemas CRISPR-Cas representam um avanço revolucionário na engenharia genética, com implicações de longo alcance em várias áreas. À medida que a pesquisa continua a revelar o pleno potencial dessa tecnologia, é essencial que os cientistas adotem práticas responsáveis que priorizem a segurança e considerações éticas. O futuro da biologia de precisão depende de nossa capacidade de aproveitar essas ferramentas poderosas enquanto navegamos em sua complexidade.
Em resumo, a tecnologia CRISPR-Cas está na vanguarda da inovação científica, com soluções transformadoras para doenças genéticas e desafios agrícolas. A pesquisa contínua e o diálogo sobre suas aplicações serão cruciais à medida que avançamos para um futuro onde a edição genética precisa se torne uma prática padrão na medicina e biotecnologia.
Referências
Doudna, J.A. e Charpentier, E., 2014. A nova fronteira da engenharia do genoma com CRISPR-Cas9. Science, 346(6213), p.1258096.
Zakrzewska, M. e Burmistrz, M., 2023. Mecanismos que regulam os sistemas CRISPR-Cas. Frontiers in Microbiology, 14, p.1060337.
Asmamaw, M. e Zawdie, B., 2021. Mecanismo e aplicações da edição do genoma mediada por CRISPR/Cas-9. Biologics: targets and therapy, pp.353-361.
Bhattacharya, S. e Satpati, P., 2022. Insights sobre o mecanismo da edição de genes baseada em CRISPR/Cas9 através de simulações de dinâmica molecular. ACS omega, 8(2), pp.1817-1837.
Castillo, A., 2016. Edição genética com CRISPR-Cas9 para o tratamento de câncer de pulmão. Colombia Médica, 47(4), pp.178-180.
Zhu, Y., 2022. Avanços no CRISPR/Cas9. BioMed Research International, 2022(1), p.9978571.
Cribbs, A.P. e Perera, S.M., 2017. Foco: Edição de genes: Ciência e bioética da edição genética CRISPR-Cas9: Uma análise para separar fatos de ficção. The Yale Journal of Biology and Medicine, 90(4), p.625.

